-
물리전자공학1 Chapter.1 요약 정리전자공학/물리전자공학1 2019. 4. 20. 19:20
물리전자공학Ⅰ 1장 요약 정리
* 결정의 종류
1) Amorphous 2) Polycrystalline 3) Single crystal
Single crystal은 하나의 경계면을 가지고 있으며 전기적 성질이 가장 뚜렷한 결정이다.* 용어
1) lattice: 결정 안에 있는 주기적인(periodic) 원자의 배열 (arrangement of atoms)을 의미.
2) lattice point: lattice 안에 있는 원자들을 표시한 점들이다.
3) lattice constant: 각 lattice point 사이의 일정한 거리를 의미한다. (a0으로 표시한다)
lattice constant의 단위는 (Å, angstrom)으로 표시하며 10-10m, 10-8cm를 의미한다.* 결정 구조 (Crystal structure)
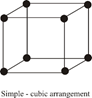
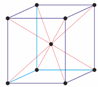
1) Simple cube


2) Body-centered cube
3) face-centered cube
4) Diamond structure
* 공간 안에 임의의 한 면(plane)이 세 축과 만나는 절편 point를 각각 p, q, s라고 하면 면을 나타내는 방법은 (1p,1q,1s )이다. 이때 p, q, s의 최소 공배수를 곱하면 (h, k, l)꼴로 나타낼 수 있다. 이 h, k, l을 우리는 Miller indices 라고 부른다.
* 면을 표현하는 방식을 (p, q, s)로 하지 않고 굳이 역수를 취해주는 이유는 다음과 같다.
만일 축에 평행한 면이 존재한다면 평행한 축과는 접점이 생기지 않으므로 infinite를 써야한다. 수식에 inf는 좋은 표기가 아니므로 역수를 취해준다면 평행한 접점에 대해서는 0으로 표기할 수 있다.* 따라서 Miller indices 방법을 사용함에 있어서 장점은 축에 평행한 면을 간단하게 표현할 수 있다는 점이다. 그러나 단점도 존재한다. 면을 표현하는 방법은 그 원점(location of origin)이 모호(entirely arbitrary)하기 때문에 cell의 모든 lattice point들은 원점이 될 수 있다는 점이 단점이다. 즉 면을 나타내는 방법은 하나지만 하나의 표현법에 대한 면의 개수는 다양하다.
예를 들어 (100) plane은 y축과 z축과 평행한 면을 의미한다.
그러나 만일 축을 90도씩 뒤틀거나 원점을 바꿔버리면 cubic의 여섯 면은 모두 (100) plane으로 나타낼 수 있다. 만일 이런 모든 면을 하나로 묶어서 나타내고 싶다면 중괄호를 사용해서 {100} plane이라고 말하면 된다. 또한 면의 방향도 고려해줘야 한다. 법선 벡터를 생각해주면 이해하기 쉽다. 한 면에 나가는 방향을 우리는 면의 방향이라고 하며 대괄호를 사용해서 [100] 이라고 한다. 앞에서 중괄호를 사용했던 것처럼 방향의 모음은 꺾쇠를 사용해서 <100>으로 표시한다.* 결정체들을 구별 짓는 2가지 중요 특징
1) 인접한 평행면까지의 거리(the distance between nearest equivalent parallel planes)(Å)
2) Surface density (단위 면적당 원자의 개수) (# of cm2)* Diamond structure은 fcc에 원자 4개가 추가된 형태이며 내부의 모든 원자는 인접한 4개의 원자들과 같은 길이로 정사면체구조로 연결돼 있다.
Diamond structure와 유사한 Zincblende structure도 있으며 두 구조 내부의 원자 구조는 사면체(Tetrahedral)라는 점이 동일하다. 차이점은 Diamond structure은 Si(실리콘)처럼 단일 원자들로 구성돼 있고 Zincblende는 GaAs(갈륨아세나이드)처럼 단일 원자들로 구성돼 있지 않다는 점이다.* 원자 결합 (Atomic Bonding)
모든 원자는 열 평형, 상온(300K)에서 총 에너지가 최소화되려는 경향으로 결합한다.
즉, 1족에 가까운 원자들은 자신의 최외각전자를 방출하려는 성향이 강하고 17족에 가까운 원자들은 최외각전자를 얻으려는 성향이 강하다. 이를 이온화(Ionize)라고 한다.* Imperfections & Impurities in solid
이론적인 single crystal structure은 이상적이지만 실제 모델은 그렇지 않다. 발생가능한 오류로는 세 가지가 있다.
1) Atomic thermal vibration 2) Point defect 3) Line defect
- Atomic thermal vibration은 모든 물질은 진동한다는 특성 때문에 일어나는 결함으로 원자들은 lattice point에 고정되어 있는 상태가 아니라 random하게 미세 운동하면서 일어나는 결함이다. 즉 lattice constant는 사실 static하지 않다.
- Point defect는 lattice point에서 발생하는 결함으로 vacancy defect와 interstitial defect로 나뉜다. Vacancy defect는 있어야할 자리에 원자가 없는 결함이고 interstitial defect는 있어서는 안되는 자리에 원자가 있는 결함을 의미한다.
- Line defect는 하나의 행 또는 열에 있는 모든 원자들이 존재하지 않는 결함을 의미한다.때로는 의도적으로 결함을 만드는 경우가 있다. Impurity를 유도하는 방법인데 이를 doping이라고 한다. 즉, 단일 원자만 들어있는 구조에 전도율을 높이기 위해 다른 종류의 원자들을 넣는 행위다. Substitutional impurity와 Interstitial impurity로 나뉘며 각각 Point defect와 대응되는 구조라고 생각하면 편하다.
- Substitutional impurity는 어느 한 Point에 있는 원자를 빼내고 다른 원자로 대체해서 집어넣는 도핑을 의미한다.
- Interstitial impurity는 있어서는 안되는 원자 자리에 외부 원자를 넣는 도핑을 의미한다.'전자공학 > 물리전자공학1' 카테고리의 다른 글
물리전자공학1 Chapter.2 요약 정리 (0) 2019.04.20